

CDE于2021年发布的指导原则《基因修饰细胞治疗产品非临床研究技术指导原则(试行)》将基因修饰细胞治疗产品定义为“经过基因修饰(如调节、替换、添加或删除等)以改变其生物学特性、拟用于治疗人类疾病的活细胞产品,如基因修饰的免疫细胞(如自然杀伤(Natural Killer, NK)细胞、树突状细胞、T细胞和巨噬细胞等),基因修饰的干细胞(如诱导多能干细胞、造血干细胞等)及其来源的细胞产品等”。其中,基因修饰的免疫细胞种类多样,具有特异性高、选择性高、毒性可控等优点,是新药研发的热门方向,在肿瘤、自身免疫性疾病等治疗领域中具有十分广阔的应用前景。本文主要介绍CAR-T、TCR-T及CAR-NK等热门基因修饰免疫细胞产品的常见临床前研究模型。
CAR-T
嵌合抗原受体T细胞(CAR-T)疗法,是利用基因工程修饰T淋巴细胞,使其表达嵌合抗原受体,以非主要组织相容性复合体(major histocompatibility complex,MHC)限制性的方式杀伤肿瘤细胞。
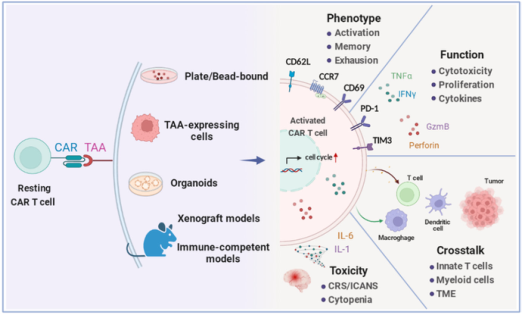
*图片来源:Si X, Xiao L, Brown CE, Wang D. Preclinical Evaluation of CAR T Cell Function: In Vitro and In Vivo Models.

*资料来源:Si X, Xiao L, Brown CE, Wang D. Preclinical Evaluation of CAR T Cell Function: In Vitro and In Vivo Models.
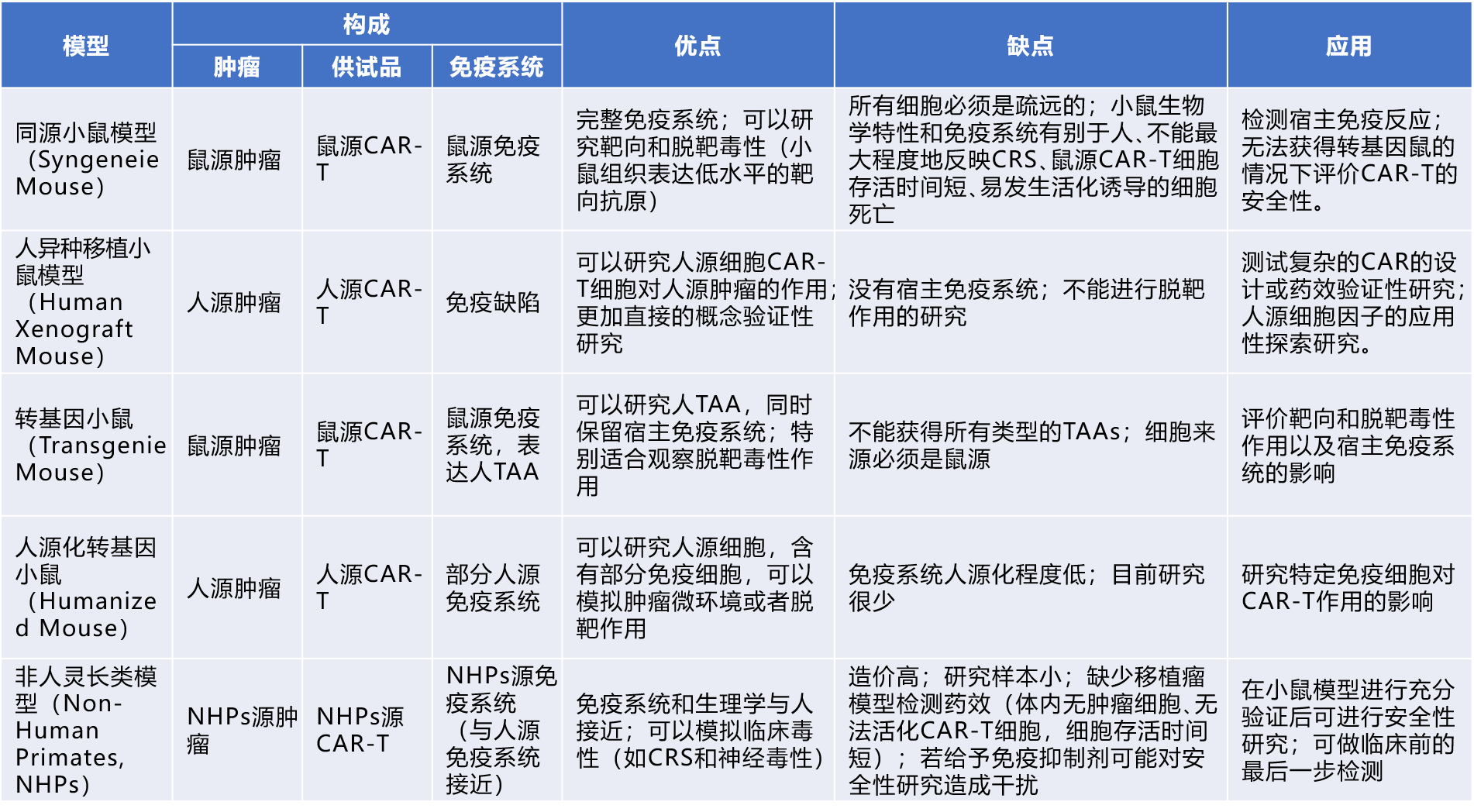
*资料来源:黄瑛, 侯田田, 霍艳. CAR-T细胞治疗产品非临床研究动物模型的发展和应用概述.
TCR-T
T细胞受体工程化T细胞(TCR-T)免疫疗法,指利用基因工程修饰T淋巴细胞,使T细胞表面表达特异性受体(T cell receptor, TCR),作为抗原识别元件,TCR能够识别更大范围的肿瘤特异性抗原,有效靶向肿瘤细胞膜表面的肽和胞内呈递的表位肽,拓宽肿瘤免疫治疗的靶点,在实体瘤中显示出非常出色的治疗效果。
CAR-NK
嵌合抗原受体NK细胞(CAR-NK)是经过基因工程修饰,能够表达嵌合抗原受体的NK细胞。由于NK细胞的独特生物学属性,CAR-NK细胞作为一种有望治疗实体瘤的细胞治疗产品,受到广泛的关注,该类产品的临床前试验模型也在不断开发和探索中。
CAR-NK已被证实可以在免疫缺陷小鼠人肿瘤异种移植模型中进行评估。为了防止宿主免疫系统消除细胞治疗效果,首选白细胞介素2受体γ链基因敲除的小鼠,例如NSG、NOG、NRG等同时缺失功能性T细胞、B细胞和NK细胞的小鼠品系,既可以保留NK活性,也可避免消除过继转移的人类效应细胞。
来自日本庆应义塾大学的研究人员成功开发了一个人源化小鼠模型——NCG-hIL15小鼠模型。该模型可以产生和维持人类NK细胞,可以表达内源性人源IL15因子,有助于人NK细胞的重建,可用于细胞功能的体内研究。马翼青等研究人员也证实了NCG-hIL15小鼠可在较长时间内维持移植入体内的人外周血NK细胞的扩增,并可以延长CAR-NK细胞的体内存活时间及维持NK细胞的杀伤功能。该模型既可用于研究人NK细胞的各种免疫学特性,也可用于荷瘤后评价CAR-NK细胞的杀伤活性,是研究人NK细胞生物学和评价CAR-NK抗肿瘤效果的有效模型。
结语
细胞和基因治疗等前沿疗法的不断涌现,对临床前研究模型提出新的要求,而借助基因工程、组织工程等领域的新技术,相关模型得以建立和优化,为创新产品的非临床有效性和安全性研究提供更适合的工具和方法,也为其临床研究提供更具价值的预测和支持。
天诚新药评价已建立成熟的细胞药物评价技术平台,能够熟练应用多种研究模型开展临床前研究,近年来已完成多种细胞治疗产品的药效学、药代动力学研究和非临床安全性评价,包括不同来源间充质干细胞(脐带、胎盘、牙髓等)、iPSCs衍生细胞、免疫细胞、3D培养细胞、干细胞外泌体等,涉及多种给药方式(静脉、皮肤、关节腔内、心肌内、鞘内等),为国内40余家知名细胞药物研发企业提供产品研发服务,帮助取得6个临床批件,多个项目即将进入临床试验注册申报阶段。
参考文献
1. Kaushik G, Venkatesha S, Verma B, Vishwakarma B, Zhang AH, Wesa A. Preclinical In Vitro and In Vivo Models for Adoptive Cell Therapy of Cancer. Cancer J. 2022 Jul-Aug 01;28(4):257-262.
2. Si X, Xiao L, Brown CE, Wang D. Preclinical Evaluation of CAR T Cell Function: In Vitro and In Vivo Models. Int J Mol Sci. 2022 Mar 15;23(6):3154.
3. Siegler EL, Wang P. Preclinical Models in Chimeric Antigen Receptor-Engineered T-Cell Therapy. Hum Gene Ther. 2018 May;29(5):534-546. doi: 10.1089/hum.2017.243. Epub 2018 Mar 14. PMID: 29390873.
4. 王琨,汪金姣,王皞鹏.T细胞受体工程化T细胞疗法的临床研究及动物肿瘤模型的应用[J].药学进展,2021,45(08):574-584.
5. Mhaidly R, Verhoeyen E. Humanized Mice Are Precious Tools for Preclinical Evaluation of CAR T and CAR NK Cell Therapies. Cancers (Basel). 2020 Jul 15;12(7):1915.
6. Katano I , Takahashi T , Ito R , et al. Predominant Development of Mature and Functional Human NK Cells in a Novel Human IL-2-Producing Transgenic NOG Mouse.[J]. The Journal of Immunology, 2015, 194(7):3513-3525.
7. 马冀青, 刘艳芳, 李恒宇,等. 人源IL-15转基因NCG小鼠在CAR-NK细胞肿瘤治疗临床前评价中的应用[J]. 中国肿瘤生物治疗杂志, 2021, 28(4):7.