

1983年外泌体于绵羊网织红细胞中被发现,1987年Johnstone将其命名为“Exosome”,但其一直被认为是一种细胞的废弃物而未受到重视。近几年,人们不断发现这种微小膜泡中含有特异性的蛋白、脂质和核酸,能作为信使携带重要的信息传递至其他细胞,从而改变其他细胞的状态或功能,这些发现让外泌体受到了越来越多的关注。本文主要对外泌体概况、提取和检测、应用领域等方面进行阐述。
1 外泌体概况
几乎所有类型的细胞均能产生外泌体,包括免疫细胞、神经细胞和干细胞等。所以,外泌体广泛存在于各种体液和组织中,如血液、唾液、尿液、肌肉组织、脂肪组织等。
1.1 外泌体的产生和作用方式
外泌体的产生过程涉及质膜的双重内陷和含有腔内囊泡的细胞内多泡体(Multivesicular bodies, MVBs)的形成。首先,细胞质膜通过内陷形成早期分选内体,包含细胞表面蛋白和细胞外成分(如蛋白质、脂质、代谢产物、小分子等)。早期分选内体与内质网、反式高尔基体和线粒体的成分可以发生融合,形成晚期分选内体。然后,晚期分选内体的双层膜内陷产生腔内囊泡,最终形成MVB。MVB可以与溶酶体或自噬体融合以被降解,也可以与细胞质膜融合,释放所含的腔内囊泡。这种被释放到细胞外,大小约为30-100nm的腔内囊泡就是外泌体。
从细胞释放的外泌体通过旁分泌以及内分泌的方式发挥作用,从而改变相邻细胞或远距离细胞的功能或状态。信号通过外泌体和细胞之间的直接融合传递,或通过结合细胞膜表面受体、内吞或吞噬作用传递。
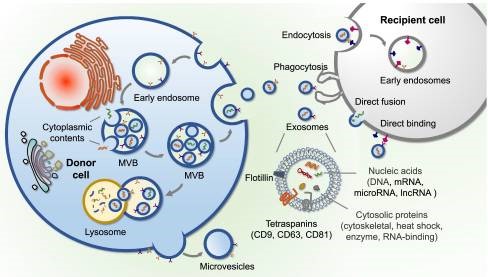
1.2 外泌体的主要组分和功能
外泌体主要是由蛋白质、脂质和核酸组成。高通量蛋白质组学分析显示,外泌体携带的蛋白质种类繁多,包括膜转运蛋白、信号转导因子、细胞骨架蛋白、跨膜蛋白、热休克蛋白等。这些蛋白在外泌体中扮演不同的角色,如细胞骨架蛋白在外泌体形成过程中起着重要作用;跨膜蛋白在细胞粘附中发挥作用;热休克蛋白参与蛋白折叠,并有助于外泌体适应细胞外环境;CD55和CD59保护外泌体不受机体免疫攻击;Alix、TSG101可作为外泌体生物标志物等。总之,不同来源的外泌体含有各自特异性蛋白质分子,而这些差异的蛋白质最终导致外泌体具有不同的生物学功能。
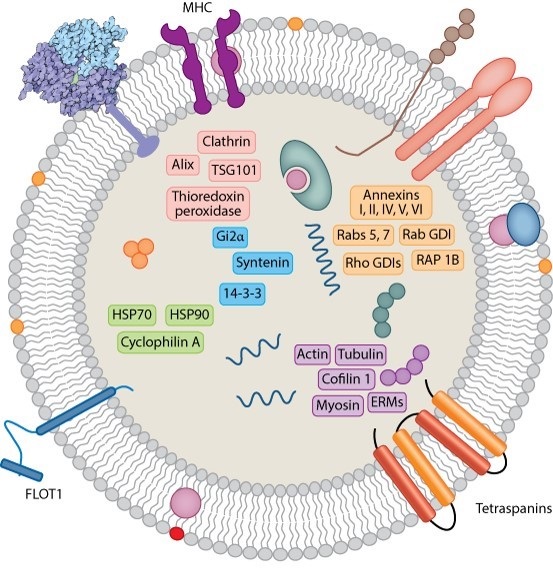
图片来源:Kourembanas S. Exosomes: vehicles of intercellular signaling, biomarkers, and vectors of cell therapy.
2 外泌体的提取及检测技术
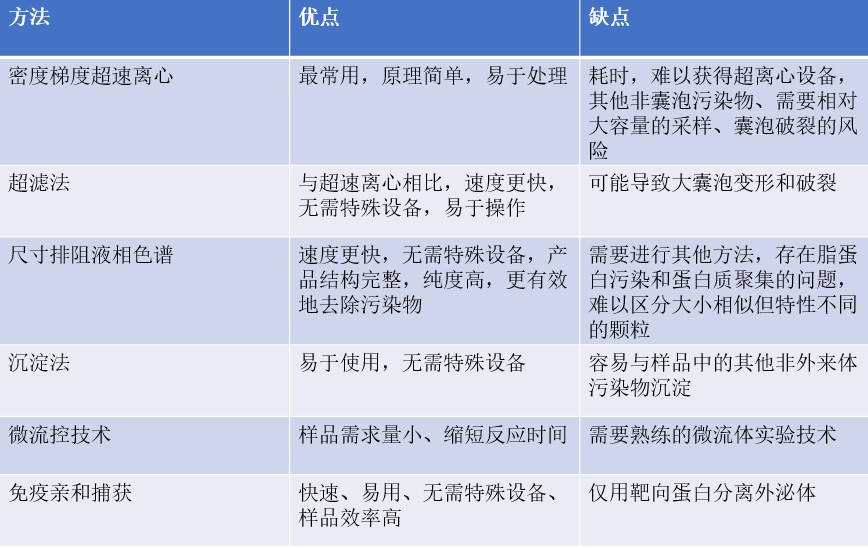
目前常用的外泌体的提取主要包括:密度梯度离心、超滤法、尺寸排阻液相色谱法、沉淀法、微流控技术和免疫亲和捕获等。不同的方法有各自的特点,选择适合的分离方法可以提高效率。下表简述了外泌体目前常用的提取方法。
对于外泌体检测,传统的方法有酶联免疫吸附法、蛋白质免疫印迹法、质谱等;新技术有纳米等离子体外泌体(Nanoplasmonic Exosome, nPLEX)传感器、集成磁-电化学外泌体(Integrated Magnetic-Electrochemical Exosome, iMEX)传感器、Exoscreen、微核磁共振、小颗粒流式细胞术等。新技术相比于传统方法,灵敏度更高,不需要太多的样本量,没有繁琐复杂的提取过程,可以运用微量样本快速获取分析结果。目前,iMEX和nPLEX均已通过大量临床研究得到验证,正在商业化;而小颗粒流式细胞术尚在发展阶段。
3 外泌体的应用
随着外泌体研究的深入,其在医疗领域得到了极大的发展,如作为生物标志物用于疾病(癌症)的诊断和预后、免疫治疗、组织修复、作为一种非细胞治疗手段进行临床治疗、作为天然药物递送载体等。
3.1 作为治疗药物
外泌体中包含多种生物因子,以及一些脂质介质和遗传物质,使得外泌体在促血管生成、抗纤维化、抗凋亡、抗炎和免疫调节方面具有治疗潜力。目前,在研的外泌体药物中,以间充质干细胞(Mesenchymal stem cells, MSCs)衍生的治疗性外泌体数量最多。临床前研究表明,间充质干细胞外泌体中天然存在的蛋白质、mRNA和miRNA可以改善衰老、损伤或病变细胞、组织和器官的功能。外泌体作为治疗药物有巨大的潜力,还需要继续探索研究。
3.2 作为诊断工具
外泌体在所有生物体液和组织中都存在,通过液体活检可以获得外泌体内容物的组成,有助于癌症的早期诊断和确定,以及疗效的预后评估等。例如,Exosome DX前列腺癌检测已被纳入美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN)指南,用于前列腺癌的早期检测。此外,疾病进展和对治疗的反应也可以通过外泌体的多组分分析来确定。外泌体诊断应用的领域包括脑血管疾病、中枢神经系统疾病和癌症,同时也迅速扩展到涉及肝脏、肾脏和肺部的其他疾病。随着研究的深入,外泌体将会应用于更多疾病的临床诊断。
3.3 作为药物递送载体
外泌体的大小与纳米颗粒相近,比腺相关病毒(Adeno-associated virus, AAVs)大,但其免疫原性和毒性更低。由病毒载体(如AAVs)递送的基因药物如果重复给药,会导致抗病毒免疫反应。纳米颗粒也是如此,人体最终会将其识别为外来物质,产生免疫反应。相比较而言,外泌体重复给药有良好的耐受性,不会产生显著的副作用。此外,有研究发现,外泌体能够跨越血脑屏障,这为向大脑输送治疗物质提供了一种方法。而且,外泌体上的CD47能帮助其避免单核细胞和巨噬细胞的吞噬作用,保护其携带药物免受吞噬,并限制它们从循环中清除。目前,外泌体作为药物载体,在核酸类药物应用领域研究最为广泛,因为其与核酸分子有很好的亲和性,能显著提高包封效率。
4 外泌体的非临床研究评价
作为新兴的研究领域,目前国内尚无相关外泌体产品专属的非临床研究指导性文件,临床前评价经验少,当作为治疗药物时,需要参考细胞治疗产品相关指导原则,如《细胞治疗产品研究与评价技术指导原则(试行)》、《免疫细胞治疗产品药效学研究与评价技术指导原则(试行)》等;若同时兼具基因产品特点,还需参考基因治疗产品相关指导原则,如《基因治疗产品非临床研究与评价技术指导原则(试行)》、《体内基因治疗产品药效学研究与评价技术指导原则(试行)》等。
5 展望与挑战
外泌体临床应用的萌芽时代正在迅速爆发。目前虽尚无获批上市的基于外泌体疗法的药物,但有进入临床阶段的药物,如Codiak Biosciences的exoSTING和exoIL-12、国内的间充质干细胞外泌体等。外泌体疗法优势明显:相比于传统药物,外泌体具有更强的靶向性和摄取性,可避免免疫排斥反应。相比于细胞药物,外泌体体积更小、更稳定、更容易修改和制造;比细胞适合长期储存、功能损失小;不会异常增殖分化,具有更高的治疗安全性。所以,外泌体有可能取代细胞治疗,并缓解血液、组织或骨髓来源的干细胞移植引起的肿瘤转化的理论问题。但目前研究也面临着诸多挑战:如外泌体难统一归类研究;各亚群之间的异质性使其质量控制难确定;天然外泌体难以体内示踪;改造后的外泌体是否会引起机体免疫反应,是否保持原有功能尚不确定;作为载体,载药效率低、目前技术手段有难度等。此外,人们对外泌体的发生机制、生物学功能等认识还不够全面,相关研究还有待继续深入开展。
参考文献:
1. Kourembanas S. Exosomes: vehicles of intercellular signaling, biomarkers, and vectors of cell therapy [J]. Annual review of physiology, 2015, 77(13-27).
2. Kalluri R,LeBleu V S. The biology, function, and biomedical applications of exosomes [J]. Science (New York, NY), 2020, 367(6478).
3. Yanez-Mo M, Siljander P R, Andreu Z, et al. Biological properties of extracellular vesicles and their physiological functions [J]. J Extracell Vesicles, 2015, 4(27066).
4. Chen B Y, Sung C W, Chen C, et al. Advances in exosomes technology [J]. Clin Chim Acta, 2019, 493(14-19).
5. Shao H, Im H, Castro C M, et al. New Technologies for Analysis of Extracellular Vesicles [J]. Chem Rev, 2018, 118(4): 1917-1950.
6. Yu D, Li Y, Wang M, et al. Exosomes as a new frontier of cancer liquid biopsy [J]. Mol Cancer, 2022, 21(1): 56.
7. Alvarez-Erviti L, Seow Y, Yin H, et al. Delivery of siRNA to the mouse brain by systemic injection of targeted exosomes [J]. Nat Biotechnol, 2011, 29(4): 341-345.