近日,贵州中观生物技术有限公司收到国家药品监督管理局签发的《药物临床试验批准通知书》,获准开展人脐带间充质干细胞注射液的1期临床试验。天诚新药评价承担了该产品药效学、药代动力学研究和非临床安全性评价等全套临床前药理毒理研究工作。
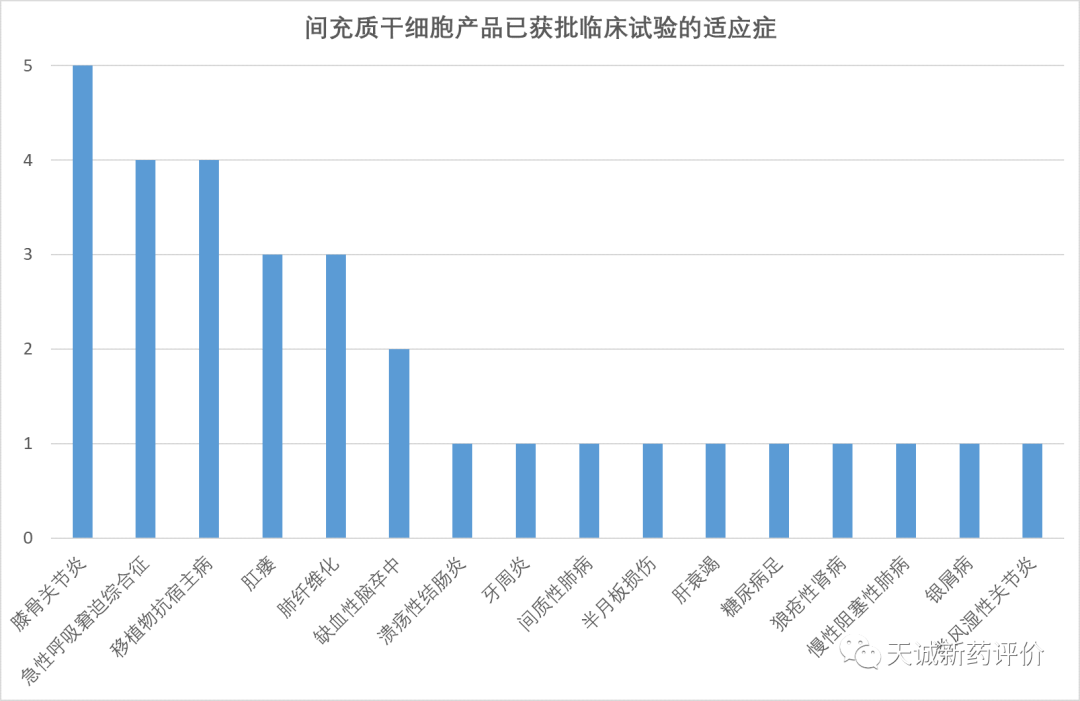
截至2022年6月21日,间充质干细胞在国内已获批临床试验共计31项,涉及16个适应症,其中:膝骨关节炎获批5项为最多,其次是急性呼吸窘迫综合征、移植物抗宿主病、肛瘘和肺纤维化。考虑到备案临床研究涉及的更多适应症,间充质干细胞的广阔应用前景可见一斑。
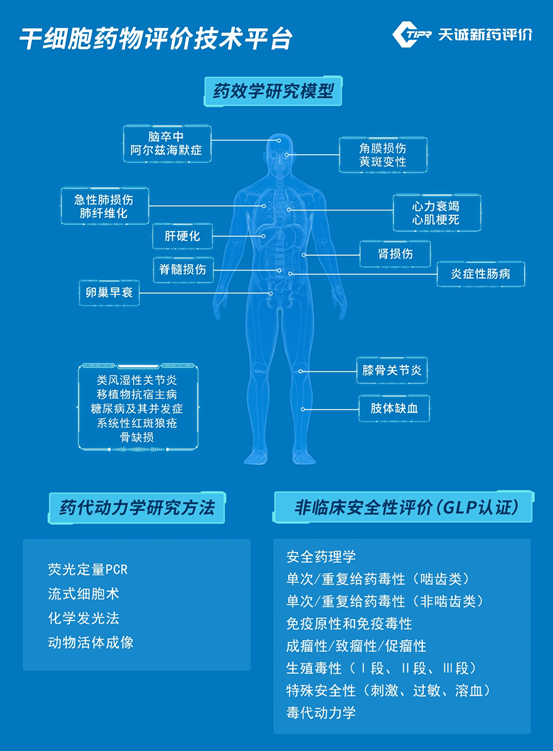
随着越来越多间充质干细胞产品获得临床试验默示许可,众多适应症扩展研究也陆续开展。天诚新药评价干细胞药物评价技术平台在药效学研究领域积累了丰富经验,建立了覆盖二十余种适应症的成熟疾病模型,结合细胞产品药代动力学研究和安全性评价体系,为超过30家细胞产品研发企业提供服务,已帮助取得5个临床试验默示许可。